Acido borico: un composto chimico dalle proprietà e usi straordinari
L’acido borico, noto anche come H3BO3 o B(OH)3, è un solido bianco cristallino sintetizzato per la prima volta da Wilhelm Homberg per acidificazione di una soluzione acquosa di borace. Il suo nome I.U.P.A.C. è triidrossidoboro.
Proprietà dell’Acido Borico
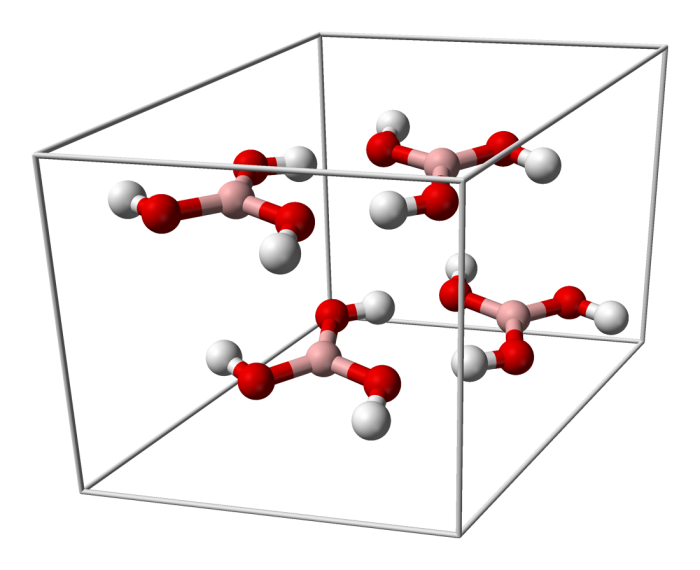
L’acido borico è scarsamente solubile in acqua a temperatura ambiente, ma si dissolve in acqua calda, etanolo e glicerolo. Presenta una struttura planare in cui il boro forma angoli di 120° con tre gruppi -OH. L’acido borico cristallino è costituito da strati di molecole legate tra loro da legami a idrogeno. Inoltre, l’acido borico non si dissocia in soluzioni acquose, ma la sua acidità è dovuta all’interazione con le molecole di acqua.
Reazioni dell’Acido Borico
Riscaldando l’acido borico a 100 °C si decompone in acido metaborico, mentre l’acido metaborico a 300 °C dà luogo alla formazione dell’acido piroborico, il quale a sua volta si decompone in ossido di boro. Inoltre, l’acido borico può essere ottenuto dalla reazione del nitruro di boro con acqua. L’acido borico si trova in natura nel minerale sassolite di origine vulcanica o lo si può ottenere da alcuni minerali contenenti borati; è contenuto nelle acque dei tessuti vegetali, animali e nell’acqua di mare.
Usi dell’Acido Borico
Nel corso dei secoli, l’acido borico è stato utilizzato per vari scopi, ma attualmente trova impiego in settori specifici. Viene impiegato in medicina come antisettico, nell’industria ceramica, nel settore del vetro per ottenere vetri con caratteristiche particolari, e nella concia delle pelli. Inoltre, è utilizzato come astringente antisettico per scottature o tagli, nel trattamento dell’acne e dei brufoli, e per soluzioni oftalmiche. Un altro importante impiego dell’acido borico è come insetticida per termiti, scarafaggi, formiche e zanzare, grazie alla sua azione disidratante che provoca una disidratazione dei parassiti.
In conclusione, l’acido borico è un composto versatile con numerose applicazioni e proprietà uniche che lo rendono prezioso in svariati settori.