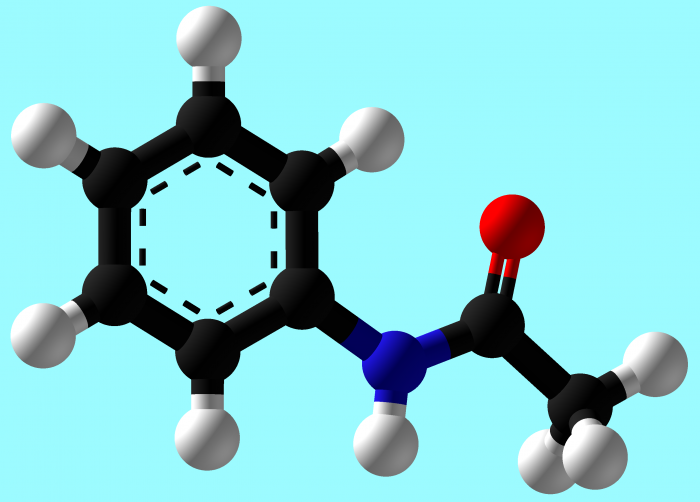
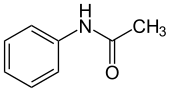
L’acetanilide il cui nome I.U.P.A.C. è N-feniletanammide è un solido poco solubile in acqua a temperatura ambiente e solubile in etanolo, etere etilico, acetone e benzene.
Ha formula C8H9NO e fu sintetizzata dal chimico statunitense Harmon Northrop Morse noto per essere stato il primo ad aver sintetizzato il paracetamolo. Si scoprì che poteva ridurre la febbre negli animali e questa scoperta suscitò l’interesse degli scienziati verso le potenziali proprietà antipiretiche del composto che tuttavia era tossico anche in dosi moderate.
Negli anni successivi, altri ricercatori continuarono gli studi sull’acetanilide e i suoi derivati. Nel 1897, il chimico francese Harmon Northrop Morse che aveva sintetizzato l’acetanilide ne modificò la struttura ottenendo il paracetamolo farmaco utilizzato a livello mondiale come analgesico e antipiretico.
Basicità
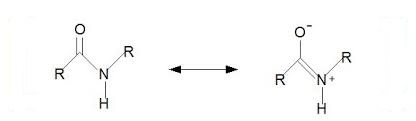
L’acetanilide è un’ammide aromatica e come le ammidi ha una bassa basicità. La debolissima basicità delle ammidi è dovuta alla natura del gruppo carbonilico che agisce da elettronattrattore. Pertanto le ammidi sono caratterizzate da due strutture limite di risonanza.
Nella seconda, che presenta separazione di carica, il doppietto elettronico solitario presente sull’azoto va a formare un doppio legame con il carbonio e l’ossigeno del gruppo carbonilico ha carica negativa contrariamente all’azoto che risulta carico positivamente.
La costante Kb è infatti dell’ordine di 10-14
Sintesi
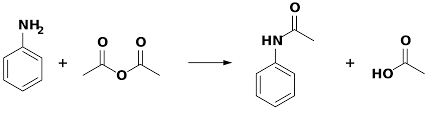
L’acetanilide viene ottenuta dalla reazione tra anilina e anidride acetica in presenza di polvere di zinco che viene utilizzato per prevenire l’ossidazione dell’anilina nel corso della reazione
Reazioni
- Nitrazione da cui si ottiene la p-nitroanilina secondo una reazione di sostituzione elettrofila aromatica.
La reazione avviene in due stadi: nel primo stadio l’acetanilide viene trattata con una miscela solfonitrica per generare in situ lo ione nitronio. In questa reazione il nucleofilo è costituito dall’anello aromatico mentre lo ione NO2+ è l’agente elettrofilo. Il maggior prodotto della reazione è la p-nitroacetanilide.
C6H5NHCOCH3 → O2NC6H4NHCOCH3
Nel secondo stadio la p-nitroacetanilide viene trattata inizialmente con acido solforico per protonare l’azoto ammidico e successivamente con NaOH con formazione di p-nitroanilina e acido acetico
- Bromurazione da cui si ottiene la p-bromoacetanilide
La reazione avviene tra bromato di potassio, acetanilide e bromuro di idrogeno:
KBrO3 + 3 C6H5NHCOCH3 + 3 HBr → 3 BrC6H4NHCOCH3 + 3 H2O + KBr
Usi
Sebbene non sia più largamente utilizzata a causa della sua tossicità è utilizzata come: