Tutto ciò che devi sapere sul furano: proprietà, sintesi e reattività
Il furano, con formula C4H4O, è un composto monociclico pentatomico contenente l’ossigeno come eteroatomo. Fu scoperto per la prima volta nel 1870 da Heinrich Limpricht, un chimico tedesco. Questa sostanza incolore è altamente volatile e infiammabile, con temperatura di ebollizione di 31°C.
Proprietà del furano
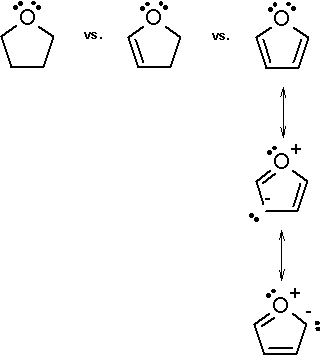
Il furano è solubile in solventi organici come etanolo, etere e acetone, ma insolubile in acqua. È importante sottolineare che è una sostanza tossica potenzialmente cancerogena. Inoltre, il furano è considerato un eterociclo aromatico a causa della delocalizzazione di uno dei due doppietti elettronici solitari dell’ossigeno all’interno dell’anello, rispettando così la regola di Hückel.
Metodi di sintesi
Il furano può essere preparato industrialmente tramite decarbonilazione catalitica del furfurolo in vapore o mediante ossidazione dell’acido furoico. Inoltre, vi sono diversi metodi importanti per ottenere derivati del furano come la sintesi di Paal-Knorr, la sintesi di Feist-Benary, la conversione di carboidrati in furani e la sintesi da enoleteri di composti β-dicarbonilici.
Reattività
Il furano dà reazioni di sostituzione elettrofila aromatica più facilmente del benzene. Molte delle reazioni tipiche come clorurazione, nitrazione, e solfonazione non sono di grande importanza pratica a causa della sensibilità del furano agli acidi forti. Il furano può anche subire una riduzione catalitica per formare il tetraidrofurano. Le reazioni con acidi minerali portano alla formazione di resine, mentre le reazioni di addizione e con dienofili sono anche comuni.
In sintesi, il furano riveste un ruolo significativo in diversi processi industriali e reazioni organiche, ed è anche presente in molti composti di origine naturale come estratti di piante e oli essenziali.