Tetrossido di osmio: caratteristiche, sintesi e reazioni
Il tetrossido di osmio, noto anche come ossido di osmio (VIII), è una sostanza chimica tossica, volatile e costosa, utilizzata come agente colorante per campioni biologici osservati al microscopio elettronico. Il vapore di tetrossido di osmio può provocare irritazioni agli occhi, alla pelle e danni polmonari.
L’osmio è un elemento di transizione con configurazione elettronica [Xe] 4f^14 5d^6 6s^2 e può presentare diversi stati di ossidazione, inclusa la forma +8 come nel caso del composto OsO4.
Proprietà e sintesi
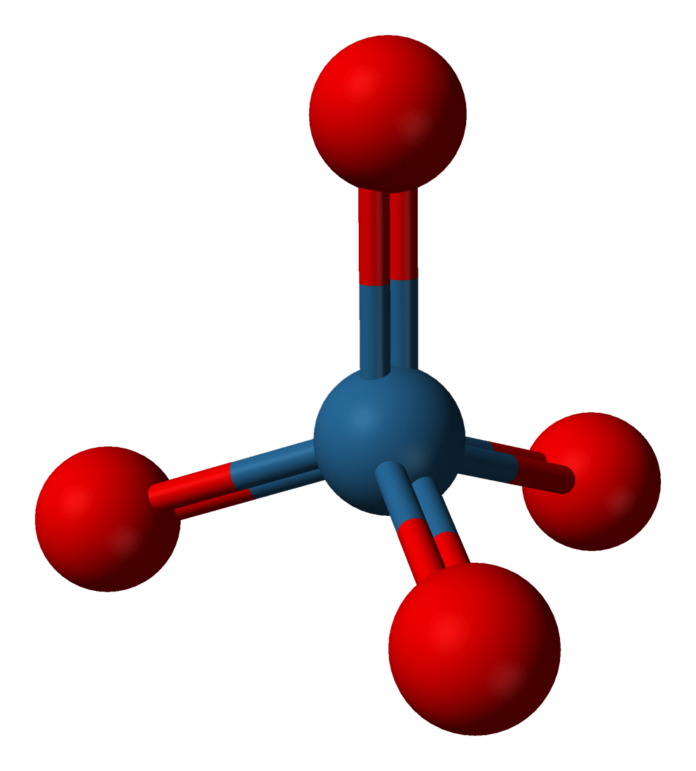
Il tetrossido di osmio ha una geometria tetraedrica con un angolo di legame O-Os-O di 109.5°, rendendo la molecola apolare. Si presenta come un solido cristallino con un punto di fusione di 40°C e un punto di ebollizione di 130°C. Va notato che la sua alta tossicità e volatilità lo rendono pericoloso se non manipolato correttamente. Nonostante sia incolore, è talvolta associato al colore giallo a causa della presenza di biossido di osmio OsO2.
La sintesi del tetrossido di osmio avviene portando il metallo alla temperatura di 400°C in presenza di ossigeno, secondo la reazione: Os + 2 O2 → OsO4. Questo composto è un acido di Lewis con proprietà ossidanti.
Reazioni e meccanismo
Il tetrossido di osmio può essere ridotto dall’idrogeno molecolare a osmio metallico attraverso la reazione: OsO4 + 4 H2 → Os + 4 H2O. È inoltre un efficace agente ossidante per la conversione di un alchene in un glicole vicinale, in una reazione stereospecifica che porta a un’addizione syn dei due gruppi –OH.
In presenza di un agente ossidante come H2O2, che rigenera l’osmio (VI) prodotto a osmio (VIII), il tetrossido di osmio viene utilizzato in quantità catalitiche per l’ossidazione degli alcheni.
Questo meccanismo di reazione prevede la formazione di un osmiato ciclico che giustifica il tipo di stereoselettività. Il tetrossido di osmio è usato principalmente come catalizzatore per l’ossidazione degli alcheni.