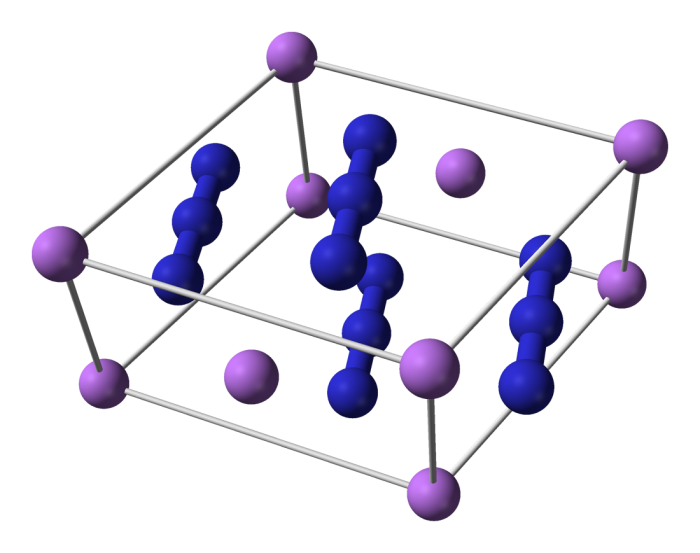
Sodio azide: dettagli sulla sintesi, le reazioni e gli usi
Il sodio azide, noto anche come azoturo di sodio, è un composto inorganico con formula NaN3, costituito dallo ione Na+ e dallo ione N3-, che può avere diverse strutture limite di risonanza. Si tratta di un sale bianco derivante dall’acido idrazoico HN3, ed è solubile in acqua e ammoniaca.
Sintesi del sodio azide
Il sodio azide può essere sintetizzato in diversi modi, tra cui la reazione tra idrazina e n-butilnitrito in ambiente basico, la reazione tra sodioammide e monossido di biazoto, e la reazione tra idrazina idrata, etilnitrito e metossido di sodio.
Reazioni
Il sodio azide è utilizzato in numerose reazioni chimiche grazie alla presenza dello ione N3-, che funge da nucleofilo. Ad esempio, la sostituzione nucleofila di un alogenuro alchilico con N3- produce un azoturo alchilico RN3, che può essere successivamente ridotto con agenti riducenti come il litio alluminio idruro o tramite idrogenazione catalitica per formare un’ammina.
In presenza di acido nitroso, il sodio azide si trasforma in azoto e monossido di azoto secondo la reazione: 2 NaN3 + 2 HNO3 → 3 N2 + 2 NO + 2 NaOH.
Usi
Il sodio azide è piuttosto stabile a condizioni normali, ma riscaldato a circa 300°C subisce una decomposizione con produzione di azoto. Questa reazione è sfruttata per rigonfiare gli airbag delle automobili, poiché il gas prodotto non è tossico.
Inoltre, utilizzando due moli di sodio azide, si ottengono tre moli di azoto gassoso, che sono sufficienti a gonfiare l’airbag. Questa reazione è sfruttata per garantire la sicurezza all’interno delle automobili.