Il flavina adenina dinucleotide è un cofattore redox di diverse reazioni importanti nel metabolismo. Questo cofattore esiste in due diversi stati di ossidazione, con FAD e FADH2 che sono rispettivamente le forme ossidate e ridotte. Può quindi partecipare a un’ampia gamma di reazioni di ossidoriduzione, nonché a reazioni mediate da liasi e transferasi.
Struttura
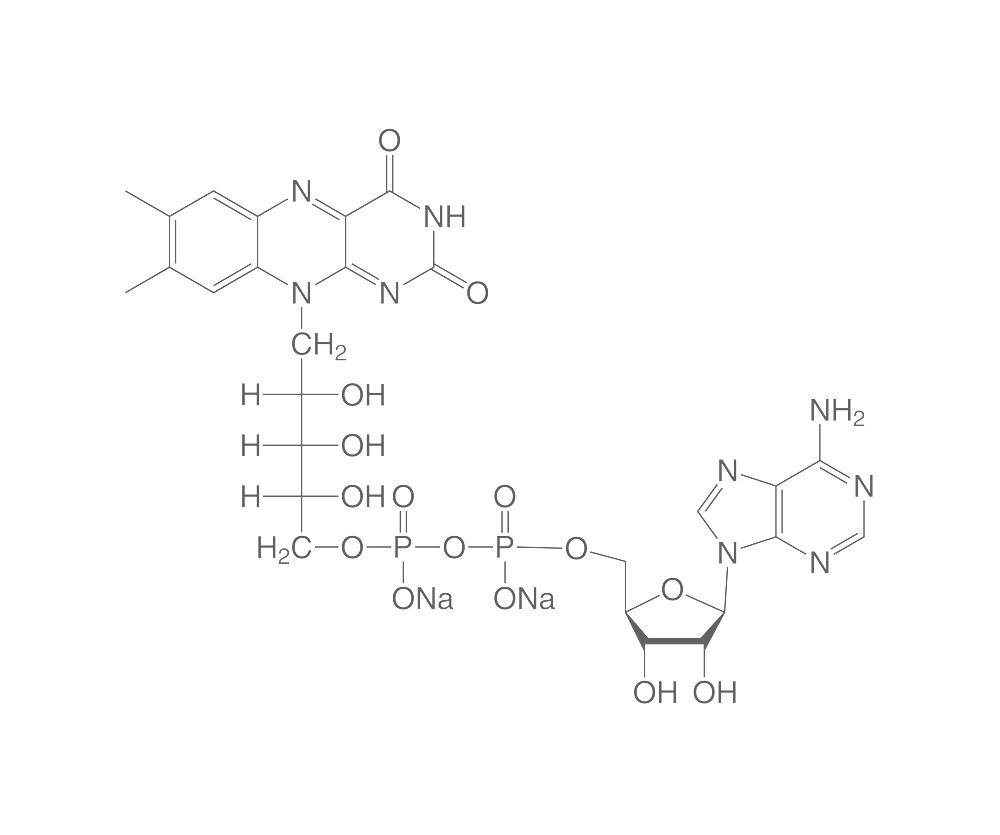
Ha formula C27H33N9O15P2 e fa parte quale gruppo protesico delle flavoproteine
Il flavina adenina dinucleotide è formato da una frazione riboflavina (vitamina B2), accoppiata a un gruppo fosfato di una molecola di ADP.
È costituita da due porzioni: l’adenina nucleotide e la flavina mononucleotide collegate tra loro attraverso i loro gruppi fosfato.
Funzioni
Il FAD è un portatore di elettroni e si riduce durante le fasi cataboliche di molecole organiche come carboidrati e lipidi. Quindi questi coenzimi ridotti possono donare questi elettroni a qualche altra reazione biochimica normalmente coinvolta in un processo anabolico (come la sintesi dell’ATP).
I flavoenzimi, che contengono FAD come gruppo protesico, catalizzano molte delle reazioni di ossidazione e di riduzione per i quattro principali sistemi di metabolismo energetico: fotosintesi, respirazione aerobica, denitrificazione e respirazione dello zolfo.
Oltre alle reazioni metaboliche il FAD partecipa a diversi processi cellulari come produzione di ROS, difesa contro lo stress ossidativo e differenziazione cellulare.
Respirazione cellulare
Un importante meccanismo nella respirazione cellulare è il trasferimento di energia al flavina adenina dinucleotide necessario a convertirla in FADH2
Infatti NAD (nicotinammide adenina dinucleotide) e il FAD svolgono un ruolo fondamentale nella respirazione grazie alla possibilità di essere ridotti a NADH e FADH2.
Nel processo di riduzione:
NADH ⇄ NAD + H+ + 1 e–
e
FADH2 ⇄ FAD + 2 H+ + 2 e–
Gli elettroni vanno a far parte della catena di trasporto degli elettroni che guida il movimento degli ioni H+ attraverso la membrana mitocondriale interna nello spazio intermembrana, creando un gradiente protonico
Il movimento degli ioni idrogeno lungo il gradiente protonico fornisce l’energia necessaria per la sintesi di ATP che è il principale trasportatore di energia dalle reazioni esoergoniche a quelle endoergoniche. Esso è quindi uno dei più importanti composti che costituisce il collegamento chimico fra catabolismo e anabolismo