Reazioni di eliminazione E1: tutto ciò che c’è da sapere
Le reazioni di eliminazione coinvolgono l’eliminazione di un protone e di un gruppo uscente da due atomi di carbonio adiacenti, creando un doppio o triplo legame.
Queste reazioni, simili alle reazioni di sostituzione nucleofila, possono avvenire attraverso la formazione di un carbocatione o tramite un meccanismo concertato.
Il termine “E1” indica Eliminazione di tipo 1, e ciò significa che la velocità della reazione è unimolecolare.
Cinetica delle reazioni E1
La velocità della reazione segue una legge cinetica del primo ordine, espressa come v = k[R-X], mostrando dipendenza del primo ordine rispetto al substrato e di ordine zero alla base.
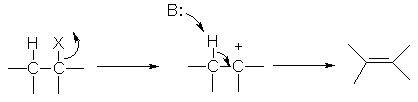
Nel meccanismo E1, la velocità della reazione è determinata dalla rottura di un legame σ e dalla formazione del carbocatione. La reazione avviene più rapidamente se il carbocatione formato è più stabile.
La base attacca l’idrogeno sul carbonio adiacente al carbocatione, che porta alla formazione del doppio legame.
Prodotti delle reazioni E1
Nelle reazioni E1 si forma l’alchene più stabile, in conformità con la regola di Zaitsev. La formazione del carbocatione può causare riarrangiamenti durante la reazione.
Il profilo della reazione mostra due stati di transizione: il primo corrisponde alla rottura del legame carbonio-gruppo uscente, mentre il secondo avviene quando la base attacca l’idrogeno per formare il doppio legame.
Le reazioni di eliminazione E1 sono influenzate dalla stabilità del carbocatione che si forma, mentre la base ha un impatto limitato sulla velocità della reazione. Tuttavia, base reattive favoriscono la formazione del prodotto di eliminazione rispetto a reazioni di sostituzione.
Per ulteriori dettagli sulle reazioni chimiche, collegati a Chimica Today.